Kronična bubrežna bolest (KBB)
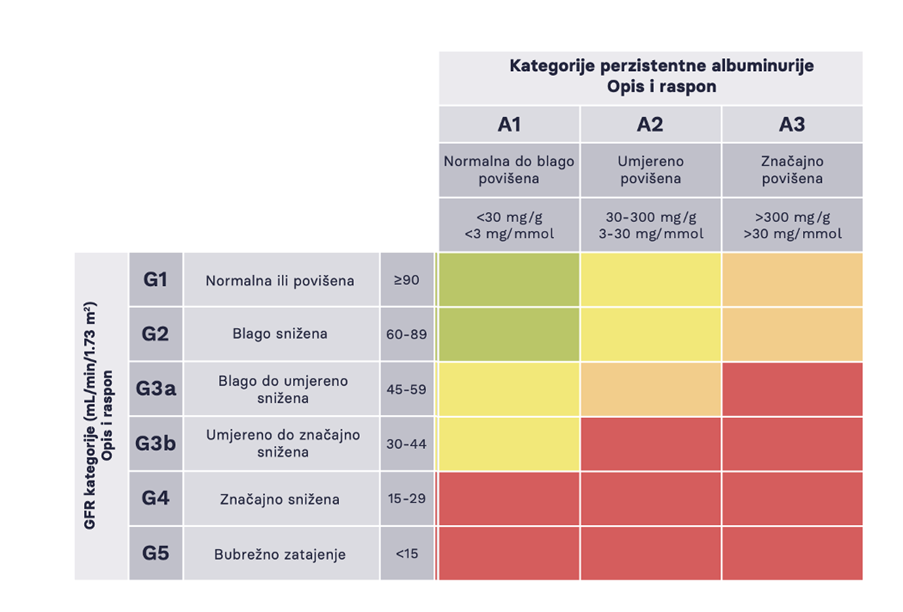
Kronična bubrežna bolest (KBB) obilježena je progresivnim smanjenjem bubrežne funkcije i/ili strukturnim promjenama unutar bubrega u trajanju od najmanje tri mjeseca. Prema KDIGO klasifikaciji, KBB se stratificira prema uzroku nastajanja, procijenjenoj glomerularnoj filtraciji (GFR) te stupnju albuminurije. Ovom klasifikacijom omogućeno je da se korištenjem jednostavnih i dostupnih parametara koji imaju značajnu kliničku važnost, vrlo lako pronađu i klasificiraju bolesnici s KBB te se procijene njihovi rizici (Slika 1).
Prevalencija KBB je u značajnom porastu te se procjenjuje da je u 2017. godini 843.6 milijuna ljudi imalo KBB, s višom prevalencijom u žena nego u muškaraca, te je kao takva jedan od vodećih uzroka smrtnosti u svijetu.(1) Među glavnim uzrocima KBB nalazi se šećerna bolest, a potom slijede arterijska hipertenzija te glomerularne bolesti. Bolesnici s KBB imaju povećani rizik za razvoj kardiovaskularnih događaja, a taj rizik je najveći kod bolesnika s višim stupnjevima KBB (stadij 4 i 5) gdje je rizik za događaje gotovo 50 %, a kardiovaskularna smrtnost uzrok je smrtnosti u gotovo 40-50 % bolesnika. Uz to, ovi bolesnici imaju i visoki rizik za razvoj aterosklerotskih komplikacija poput infarkta miokarda, moždanog udara, srčanog popuštanja te razvoja fatalnih aritmija.(2)
Upravo zbog ovakvog visokog rizika za razvoj kardiovaskularnih događaja i njihovih komplikacija, te povećane smrtnosti, potrebna je brza identifikacija bolesnika s KBB te njihovo pravovremeno praćenje i liječenje primjenom organoprotektivnih lijekova s dokazanom učinkovitosti, te agresivna kontrola svih dodatnih rizičnih faktora, poput optimalne kontrole arterijskog tlaka, adekvatne kontrole dislipidemije te dobre kontrole šećerne bolesti. Upravo sa ovakvim pristupom može se usporiti progresija KBB te smanjiti kardiovaskularne događaje u ove visoko rizične skupine bolesnika.
Uloga mineralokortikoidnih receptora u razvoju KBB te važnost njihove blokade
Mineralokortikoidni receptori (MR) pripadaju podskupini nuklearnih hormonskih receptora koji se nalaze u brojnim tkivima, poput bubrega, srca, imunološkim stanicama, živčanom sustavu. Njihova glavna uloga je u regulaciji homeostaze ekstracelularne tekućine, ali i elektrolita i arterijskog tlaka. Aldosteron, kao glavni ligand za MR stvara se u nadbubrežnim žlijezdama te djeluje i na epitelne i ne-epitelne stanice.
U KBB dolazi do patološke i pretjerane aktivacije mineralokortikoidnih receptora što dovodi do progresije kronične bubrežne bolesti putem podržavanja i poticanja upale i fibroze. Ovakvi štetni učinci nisu ograničeni samo na bubreg, već zahvaćaju i kardiovaskularni sustav dovodeći do remodeliranja miokarda i nastanka vaskularne disfunkcije. Sama aktivacija mineralokortikoidnih receptora u bubrezima dovodi do oštećenja podocita, potiče oksidativni stres koji utječe na endotel pri čemu se razvija i endotelna disfunkcija. Također, aldosteron u bubregu potiče reapsorpciju natrija i izlučivanje kalija dovodeći do retencije tekućine i time potiče razvoj arterijske hipertenzije.
Upravo zbog ove pretjerane aktivacije mineralokortikoidnih receptora koja je prisutna u KBB, jasno je da blokada ovih receptora predstavlja racionalnu terapijsku opciju s ciljem usporavanja progresije kronične bubrežne bolesti, ali i smanjenja kardiovaskularnih neželjenih događaja koji su prisutni u ovih, visokorizičnih bolesnika.(3,4)
Dokazi o učinkovitosti MRA terapije
Brojna randomizirana kontrolirana ispitivanja pokazala su da primjena antagonista mineralokortikoidnih receptora (MRA), bilo kao monoterapija ili u kombinaciji sa inhibitorima renin-angiotenzinskog sustava (ACEI/ARB) značajno smanjuju proteinuriju, omjer albumin/kreatinina u urinu (uACR) te da imaju i antiproteinurični učinak u glomerularnim bolestima.(4) Meta-analiza 31 studije koja je obuhvatila prve generacije MRA, spirinolaktona i eplerenona, pokazala je smanjenje albuminurije za 24,55 % i proteinurije za 53,93 %.(5)
Unatoč ovim snažnim dokazima o učinkovitosti MRA njihova primjena u kliničkoj praksi je i dalje niska, te dominantno rezervirana za bolesnike koji imaju znakove srčanog popuštanja. Glavni razlog ovakve kliničke inercije nalazi se u strahu od nuspojava, ponajprije hiperkalemije. Međutim, uz odgovarajući nadzor, prilagodbu doze te primjenu dodatnih terapijskih mjera, poput diuretika ili vezača kalija, rizik se u velikom broju slučajeva može uspješno kontrolirati, pogotovo ako uzmemo u obzir važnost blokade mineralokortikoidnih receptora u progresiji KBB.
Upravo zbog sigurnosnih ograničenja steroidnih MRA, recentno su razvijeni i nesteroidni antagonisti mineralokortikoidnih receptora, među kojima je trenutno najviše ispitan finerenon. Trenutno je njegova glavna terapijska opcija u bolesnika s KBB i šećernom bolesti tip II kod kojih je pokazao značajan nefroprotektivni učinak, uključujući smanjenje albuminurije, usporavanje progresije bubrežne bolesti te smanjenje kardiovaskularnih događaja.(6)
Na temelju dostupnih dokaza, u današnje vrijeme se u bolesnika sa šećernom bolesti i KBB sve češće govori o četiri temeljna stupa nefroprotekcije: inhibitori renin-angiotenzinskog sustava, SGLT2 inhibitori, nesteroidni MRA te GLP-1 receptor agonisti. Rano, pravovremeno i kombinirano uvođenje ova četiri stupa osigurava se optimalna nefroprotekcija te postiže smanjenje albuminurije i usporavanje progresije kronične bubrežne bolesti, a istodobno se djeluje povoljno na kardiovaskularni sustav.
Zaključak
Kronična bubrežna bolest predstavlja značajan javnozdravstveni problem koji često ostaje neprepoznat u ranim fazama zbog oskudnih simptoma, unatoč visokim kardiovaskularnim rizicima. Stoga je odgovornost svih sudionika zdravstvenog sustava ključna za rano otkrivanje rizičnih bolesnika, poput onih sa šećernom bolesti, arterijskom hipertenzijom ili onih sa srčanim popuštanjem. Pri tome nam kao jednostavni i dostupni alati na raspolaganju stoji procjena bubrežne funkcije primjenom GFR-a te uACR-a prema važećoj KDIGO klasifikaciji čime se lagano mogu klasificirati bolesnici koji zahtijevaju praćenje i adekvatno liječenje.
Dostupni dokazi jasno pokazuju da suvremena organoprotektivna terapija koja uključuje blokadu renin-angiotenzinskog sustava, SGLT2 inhibitore te selektivne i neselektivne MRA, može značajno usporiti progresiju kronične bubrežne bolesti te smanjiti kardiovaskularni mortalitet. Zaboravljanje MRA terapije u liječenju KBB danas nije više pitanje nedostatka dokaza već postojanja kliničke inercije na koju svi osobno možemo utjecati.
- Kovesdy CP. Epidemiology of chronic kidney disease: an update 2022. Kidney Int Suppl (2011). 2022 Apr;12(1):7-11. doi: 10.1016/j.kisu.2021.11.003. Epub 2022 Mar 18. PMID: 35529086; PMCID: PMC9073222.
- Jankowski J, Floege J, Fliser D, Böhm M, Marx N. Cardiovascular Disease in Chronic Kidney Disease: Pathophysiological Insights and Therapeutic Options. Circulation. 2021 Mar 16;143(11):1157-1172. doi: 10.1161/CIRCULATIONAHA.120.050686. Epub 2021 Mar 15. PMID: 33720773; PMCID: PMC7969169.
- Epstein M, Kovesdy CP, Clase CM, Sood MM, Pecoits-Filho R. Aldosterone, Mineralocorticoid Receptor Activation, and CKD: A Review of Evolving Treatment Paradigms. Am J Kidney Dis. 2022 Nov;80(5):658-666. doi: 10.1053/j.ajkd.2022.04.016. Epub 2022 Sep 1. PMID: 36057467.
- Barrera-Chimal J, Jaisser F, Anders HJ. The mineralocorticoid receptor in chronic kidney disease. Br J Pharmacol. 2022 Jul;179(13):3152-3164. doi: 10.1111/bph.15734. Epub 2021 Dec 28. PMID: 34786690.
- Alexandrou M, Papagianni A, Tsapas A, Loutradis C, Boutou A, Piperidou A, et al. Effects of mineralocorticoid receptor antagonists in proteinuric kidney disease: A systematic review and meta-analysis of randomized controlled trials. J Hypertens. (2019) 37:2307–24. 10.1097/HJH.0000000000002187[DOI] [PubMed] [Google Scholar][Ref list]
- Bakris GL, Agarwal R, Anker SD, Pitt B, Ruilope LM, Rossing P, Kolkhof P, Nowack C, Schloemer P, Joseph A, Filippatos G; FIDELIO-DKD Investigators. Effect of Finerenone on Chronic Kidney Disease Outcomes in Type 2 Diabetes. N Engl J Med. 2020 Dec 3;383(23):2219-2229. doi: 10.1056/NEJMoa2025845. Epub 2020 Oct 23. PMID: 33264825.


Komentiranje je dozvoljeno samo registriranim korisnicima. Svaki korisnik koji želi komentirati članke obvezan je prethodno se upoznati s Pravilima komentiranja na belupoint.hr.