Uvod
Infarkt miokarda označava visoki rizik za ponovne kardiovaskularne događaje i smrtnost.
Sekundarna prevencija nakon infarkta uključuje kombinaciju promjena životnog stila, kardiovaskularne rehabilitacije i optimalne farmakoterapije, u kojoj statini igraju ključnu ulogu zbog sposobnosti značajnog smanjenja LDL-kolesterola i time smanjenja rizika od ponovnog infarkta i drugih kardiovaskularnih događaja.
Zašto intenzivna (visoka doza) statinska terapija?
- Statini smanjuju sintezu kolesterola inhibicijom HMG-CoA reduktaze, što dovodi do pada LDL-kolesterola i stabilizacije aterosklerotskih plakova.
- Nakon infarkta miokarda cilj je brzo i trajno smanjiti aterotrombotski rizik. Veće smanjenje LDL-a korelira s većim apsolutnim i relativnim smanjenjem rizika za buduće kardiovaskularne događaje.
- Europske smjernice i kliničke preporuke ističu primjenu visokih doza statina u sekundarnoj prevenciji kako bi se postigla značajna redukcija LDL-a i bolji klinički ishodi kod bolesnika nakon preboljelog infarkta miokarda.
- Među statinima, atorvastatin je postao prva linija liječenja zahvaljujući svojoj dokazanoj učinkovitosti u smanjenju LDL-kolesterola i povoljnim kliničkim ishodima povezanim ne samo uz sniženje LDL-a.
Preporuka visokointenzivne terapije
Europsko kardiološko društvo preporučuje početnu visoku dozu atorvastatina od 80 mg odmah nakon akutnog infarkta miokarda (razina preporuke IA), uz kasnije održavanje visokointenzivne doze prema vrijednostima LDL-a, radi trajne sekundarne prevencije.
U praksi to obično znači početak terapije visokim dozama atorvastatina već u bolnici te prilagodbu doze prema postignutom LDL-u i podnošljivosti lijeka.
Rosuvastatin u visokoj dozi — kako odabrati statin?
U posljednje vrijeme sve se češće u terapiju nakon infarkta miokarda uvodi rosuvastatin u visokoj dozi. Budući da su na raspolaganju dva visokopotentna statina novije generacije, nameće se pitanje koji statin odabrati.
Head-to-head usporedba
Evo pregledne head‑to‑head tablice s fokusom na koronarne bolesnike, temeljene na navedenim izvorima i ključnim smjernicama:
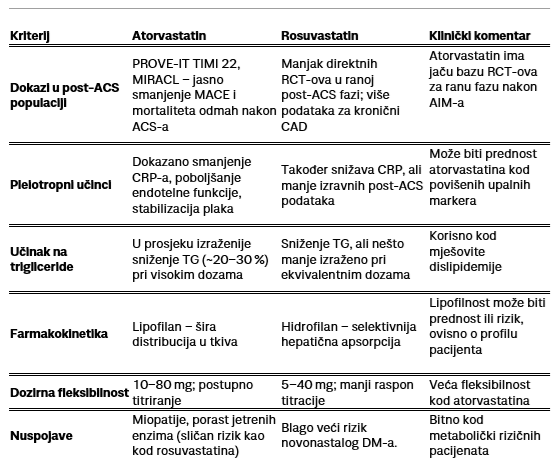
Zaključak:
Cilj visokointenzivne statinske terapije jest rano i agresivno snižavanje LDL-a nakon infarkta miokarda te smanjenje neželjenih kardiovaskularnih događaja.
Pleiotropni učinci dodatno nadopunjuju klasično snižavanje LDL-kolesterola te pojačavaju zaštitu bolesnika od ponovnih ishemijskih događaja i progresije ateroskleroze.
Atorvastatin za navedeno ima snažniji temelj u RCT-ovima.
Oba statina (atorvastatin i rosuvastatin) snižavaju CRP i poboljšavaju endotelnu funkciju, no atorvastatin je prema nekim parametrima bolje ocijenjen:
- snažnije snižava ekspresiju proinflamatornih citokina (IL-6, TNF-α), smanjuje kroničnu upalu u vaskularnom zidu i stvaranje reaktivnih kisikovih spojeva
- jače inhibira metaloproteinaze i smanjuje infiltraciju makrofaga, čime se smanjuje rizik rupture vulnerabilnih lezija
- blokira proliferaciju glatkih mišićnih stanica i smanjuje fibrotične promjene u stijenkama krvnih žila te prevenira negativne promjene u srčanom mišiću nakon ishemijskog oštećenja
Rosuvastatin je izvrstan izbor za postizanje vrlo niskih vrijednosti LDL-a uz manju dozu, no u post-ACS kontekstu atorvastatin ostaje „prvi među jednakima” prema dostupnim dokazima.
Atorvastatin u prosjeku snažnije snižava TG-a.
Profil nuspojava je sličan, uz nešto veći rizik novonastalog DM-a kod rosuvastatina u nekim studijama.
Ukupno gledajući, navedeni pleiotropni učinci dopunjuju učinak na snižavanje LDL-kolesterola i pojačavaju zaštitu bolesnika od ponovnih ishemijskih događaja i progresije ateroskleroze.
Stoga bih u izboru statina za visokointenzivnu hipolipemijsku terapiju nakon infarkta miokarda dao prednost atorvastatinu.
- European Society of Cardiology. 2019 ESC Guidelines for the diagnosis and management of chronic coronary syndromes. Eur Heart J. 2020;41(3):407–477.
- Mirjanić-Azarić B, Jelić-Ivanović Z, Zeljković A, et al. Pleiotropic effects of atorvastatin on stable angina patients: evidence by analysis of HDL size and subclasses, and plasma mRNA. J Med Biochem. 2015;34(3):314–322. (analizirane su promjene u veličini i raspodjeli HDL subfrakcija te ekspresija tri ključna gena u plazmi (ICAM-1, CCL2 i katepsin S), čime su potvrđeni antiinflamatorni i antioksidativni učinci lijeka.
- ARMYDA Investigators. Atorvastatin reload before elective percutaneous coronary intervention reduces periprocedural myocardial injury and inflammation. J Am Coll Cardiol. 2004;44(5):986–992.
- PROVE-IT TIMI 22 Investigators. Intensive versus moderate lipid lowering with statins after acute coronary syndromes. N Engl J Med. 2004;350(15):1495–1504.
- TNT (Treating to New Targets) Investigators. Intensive lipid lowering with atorvastatin in patients with stable coronary disease. JAMA. 2001;285(20):1711–1718.
- MIRACL Study Group. Early atorvastatin treatment improves outcomes in acute coronary syndromes: results of the MIRACL trial. JAMA. 2001;285(20):1711–1718.
- Atorvastatin u sekundarnoj prevenciji akutnog koronarnog sindroma. JGL Kutak za stručnjake. 2021.
- Libby P, Ridker PM, Hansson GK. “Progress and challenges in translating the biology of atherosclerosis.” Nature. 2011;473(7347):317–325.
- Ridker PM, et al. “Rosuvastatin to prevent vascular events in men and women with elevated C-reactive protein (JUPITER Trial).” N Engl J Med. 2008;359(21):2195–2207.
- Amarenco P, et al. “High-dose atorvastatin after stroke or transient ischemic attack (SPARCL Trial).” Lancet. 2006;367(9507):1711–1720.
- Liao JK. “Isoprenoids as mediators of the biological effects of statins.” Journal of Clinical Investigation. 2002;110(3):285–288.
- Jain MK, Ridker PM. “Anti-inflammatory effects of statins: clinical evidence and basic mechanisms.” Nature Reviews Drug Discovery. 2005;4(12):977–987.
- Sahebkar A, et al. “Pleiotropic effects of statins: an updated meta-analysis of randomized clinical trials.” Pharmacological Research. 2016;111:675–687.
- European Society of Cardiology/European Atherosclerosis Society.



Komentiranje je dozvoljeno samo registriranim korisnicima. Svaki korisnik koji želi komentirati članke obvezan je prethodno se upoznati s Pravilima komentiranja na belupoint.hr.