Uvod
Oralna antikoagulantna terapija (OAK) temelj je prevencije i liječenja tromboembolijskih događaja u bolesnika s fibrilacijom atrija, venskom tromboembolijom i mehaničkim srčanim valvulama. U kliničkoj praksi primjenjuju se antagonisti vitamina K (VKA) i direktni oralni antikoagulansi (DOAK). Perioperativno upravljanje OAK-om zahtjeva individualiziranu procjenu tromboembolijskog i hemoragijskog rizika, uzimajući u obzir vrstu zahvata, farmakokinetiku lijeka i bubrežnu funkciju bolesnika. Cilj ovog rada je prikazati suvremene preporuke za vođenje OAK-a s posebnim naglaskom na režime prekida i ponovnog uvođenja terapije prije i nakon invazivnih zahvata.
Tromboembolijske bolesti predstavljaju značajan uzrok morbiditeta i mortaliteta. Uvođenje direktnih oralnih antikoagulansa promijenilo je kliničku praksu zahvaljujući predvidljivijem farmakodinamskom profilu i manjoj potrebi za laboratorijskim nadzorom u odnosu na VKA. Međutim, perioperativno razdoblje i dalje predstavlja klinički izazov zbog potrebe balansiranja između rizika tromboze i rizika krvarenja.
Farmakološke osnove oralne antikoagulantne terapije
Najzastupljeniji predstavnik VKA jest varfarin. Karakterizira ga djelovanje na više razina koagulacijske kaskade (inhibicija sinteze II, VII, IX i X faktora te proteina C i S). Specifičnost je i tzv. uski terapijski prozor (definiran kao vrijednosti INR 2,0-3,5) koji je često puta u kliničkoj praksi teško postići zbog višestrukih razloga (farmakokinetika, interakcija s lijekovima/hranom). U novije vrijeme VKA su gotovo upotpunosti zamijenili direktni oralni antikoagulansi, prvenstveno zbog boljeg sigurnosnog profila, ali i jednostavnijeg terapijskog režima koji doprinosi boljoj suradljivosti bolesnika, a time i učinkovitosti same terapije. Jedina indikacijska područja gdje su VKA još uvijek zlatni standard u liječenju su bolesnici s ugrađenim mehaničkim zaliscima i trombofilijama (primjerice antifosfolipidni sindrom).
Kada govorimo o DOAK, njih dijelimo na dvije skupine: inhibitori faktora IIa (dabigatran) i faktora Xa (rivaroksaban, apiksaban, edoksaban). Karakterizira ih brzi početak djelovanja (2–4 sata), kraće poluvrijeme eliminacije (8–15 sati) te predvidljiv antikoagulantni učinak bez potrebe za rutinskim laboratorijskim praćenjem. Svakako treba reći da i ovdje postoje određena klinička ograničenja (značajno narušena bubrežna funkcija <15ml/min, tjelesna masa <50kg, BMI >40kg/m2, mehanički zalisci) koja zahtjevaju individualiziran pristup bolesniku.
Procjena rizika prije zahvata
Prilikom procjene rizika važno je stratificirati bolesnika prema tromboembolijskom riziku, kao i riziku od značajnijeg kliničkog krvarenja. Glede tromboembolijskih rizika, najčešće u obzir uzimamo tzv. kalkulatore rizika (npr. CHA₂DS₂-VA) kojima pokušavamo odrediti godišnji rizik pojavnosti moždanog udara kod takve populacije. Sukladno tome procjenjujemo koliko je sigurno kratkotrajno obustaviti OAK. Od ostalih kliničkih parametara svakako uzimamo u obzir podatak o recentnom preboljenju venskog tromboembolizma (VTE), ugradbenim mehaničkim zaliscima ili trombofilijama. U slučaju postojanja navedenog, određuje se modalitet antikoagulancije neposredno prije samog zahvata, tijekom samog zahvata, kao i uvođenje nekog oblika trajne OAK (najčešće vraćanje ‘stare’) po završetku liječenja (u kliničkoj praksi to nazivamo ‘bridging’ terapija).
Kod procjene rizika od značajnog kliničkog krvarenja, uzimamo u obzir činjenicu o kojem se zahvatu točno radi, budući da ne nose svi zahvati jednak rizik krvarenja.
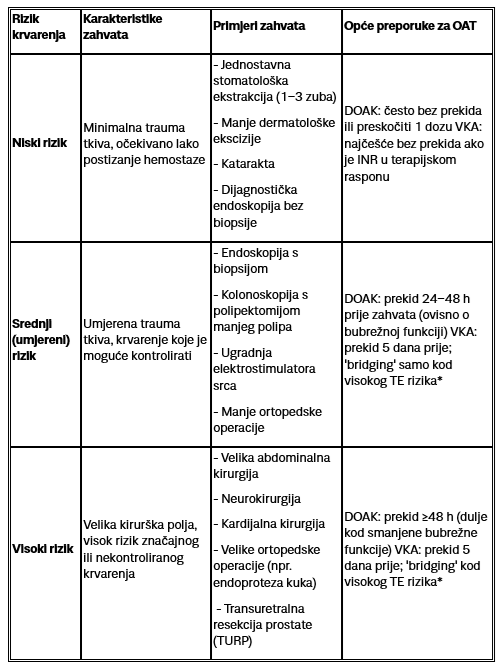
Hitni zahvati i reverzija antikoagulacije
U slučaju životno ugrožavajućih stanja kod velike većine bolesnika indicirana je žurno poništavanje antikoagulancije. Kod VKA i dabigatrana postoje dobra terapijska rješenja koja vrlo brzo i učinkovito (2-30min) poništavaju efekt antikoagulancije, dok za inhibitore Xa faktore ne postoje specifični antidoti. Svakako treba istaknuti da je kod liječenja takvih bolesnika također ključno i suportivno liječenje (nadomjesno liječenje kristaloidima, transfuzijski suport).
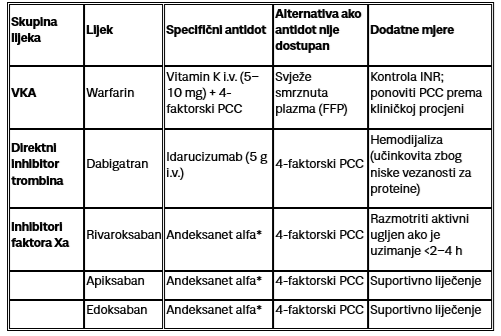
Regionalna anestezija
Kod spinalne ili epiduralne anestezije potrebno je strogo poštivati vremenske intervale prekida terapije zbog rizika spinalnog hematoma, sukladno važećim anesteziološkim smjernicama.
Zaključak
Perioperativno upravljanje oralnom antikoagulantnom terapijom zahtijeva individualizirani, strukturirani pristup temeljen na procjeni tromboembolijskog i hemoragijskog rizika. DOAK-ovi su pojednostavili perioperativno vođenje zahvaljujući kraćem poluvremenu i izostanku potrebe za ‘bridging’ terapijom u većini slučajeva. S druge strane, bolesnici na VKA terapiji, osobito s mehaničkim valvulama ili nedavnom tromboembolijom, zahtijevaju pažljivo planiranje i često primjenu ‘bridging’ terapije. Multidisciplinarna suradnja ostaje ključna za sigurnost bolesnika i optimalne kliničke ishode.
- European Society of Cardiology. 2020 ESC Guidelines for the diagnosis and management of atrial fibrillation developed in collaboration with EACTS. Eur Heart J. 2020;42(5):373–498.
- European Society of Cardiology. 2021 ESC Guidelines on cardiovascular disease prevention in clinical practice. Eur Heart J. 2021;42(34):3227–3337.
- American College of Chest Physicians. Perioperative management of antithrombotic therapy: CHEST guideline and expert panel report. Chest. 2022;162(5):e207–e243.
- European Heart Rhythm Association Practical guide on the use of non-vitamin K antagonist oral anticoagulants in patients with atrial fibrillation. Eur Heart J. 2021;42(40):3731–3742.
- Douketis JD, Spyropoulos AC, Murad MH, Arcelus JI, Dager WE, Dunn AS, et al. Perioperative management of antithrombotic therapy. Chest. 2022;162(5):e207–e243.
- Steffel J, Verhamme P, Potpara TS, Albaladejo P, Antz M, Desteghe L, et al. The 2021 EHRA Practical Guide on the use of non-vitamin K antagonist oral anticoagulants in patients with atrial fibrillation. Eur Heart J. 2021;42(40):3731–3742.
- American Heart Association. 2019 AHA/ACC/HRS focused update on atrial fibrillation. Circulation. 2019;140(2):e125–e151.
- Connolly SJ, Ezekowitz MD, Yusuf S, Eikelboom J, Oldgren J, Parekh A, et al. Dabigatran versus warfarin in patients with atrial fibrillation. N Engl J Med. 2009;361:1139–1151.
- Patel MR, Mahaffey KW, Garg J, Pan G, Singer DE, Hacke W, et al. Rivaroxaban versus warfarin in nonvalvular atrial fibrillation. N Engl J Med. 2011;365:883–891.
- Granger CB, Alexander JH, McMurray JJV, Lopes RD, Hylek EM, Hanna M, et al. Apixaban versus warfarin in patients with atrial fibrillation. N Engl J Med. 2011;365:981–992.
- Giugliano RP, Ruff CT, Braunwald E, Murphy SA, Wiviott SD, Halperin JL, et al. Edoxaban versus warfarin in patients with atrial fibrillation. N Engl J Med. 2013;369:2093–2104.
- Pollack CV Jr, Reilly PA, Eikelboom J, Glund S, Verhamme P, Bernstein RA, et al. Idarucizumab for dabigatran reversal. N Engl J Med. 2015;373:511–520.



Komentiranje je dozvoljeno samo registriranim korisnicima. Svaki korisnik koji želi komentirati članke obvezan je prethodno se upoznati s Pravilima komentiranja na belupoint.hr.