Uvod
Epilepsija je kronična neurološka bolest koja se javlja u oko 1 % populacije. Procjenjuje se da u svijetu oko 50 milijuna ljudi boluje od epilepsije.
Unatoč brojnim mogućnostima farmakoterapije i dostupnosti stare i nove generacije antiepileptika, još uvijek 20–30 % oboljelih nema dobro kontroliranu bolest, odnosno i dalje imaju različitu učestalost epileptičkih napadaja. Ta skupina bolesnika svrstava se u farmakorezistentnu epilepsiju i postaje kandidat za neku od drugih metoda liječenja.
Tu prije svega spadaju određene neurokirurške metode. Te metode mogu biti kurativne, poput resektivne neurokirurgije, ili palijativne, koje uključuju neuromodulacijske metode te invazivnije zahvate poput korpus kalozotomije, diskonekcije ili hemisferektomije.
U neuromodulacijske metode liječenja epilepsije ubrajaju se ugradnja stimulatora živca vagusa (VNS), duboka mozgovna stimulacija (DBS) i responsivna neurostimulacija (RNS). Navedene metode primjenjuju se ovisno o vrsti epilepsije i epileptičkih napadaja, ali i o dostupnosti te cijeni pojedine metode.
Stimulacija n. vagusa (VNS)
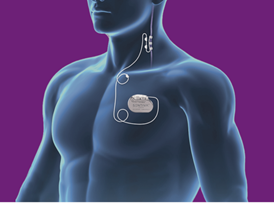
Ugradnja stimulatora živca n. vagusa (VNS) koristi se u liječenju farmakorezistentne epilepsije od 1997. godine. Riječ je o metodi pri kojoj se elektroda postavlja oko lijevog n. vagusa i spaja s generatorom koji se implantira u području prsnog koša, ispod klavikule, tj. ispod pektoralnog mišića. Stimulacija se obično provodi putem lijevog n. vagusa jer desni n. vagus, za razliku od lijevog, inervira sinoatrijski (SA) čvor, pa postoji veći rizik od srčanih aritmija.
Točan mehanizam djelovanja VNS-a još uvijek nije u potpunosti poznat. Postoji nekoliko teorija koje objašnjavaju kako VNS dovodi do smanjenja epileptičkih napadaja. Povremene stimulacije n. vagusa putem njegovih eferentnih vlakana potiču aktivaciju jezgri u moždanom deblu, prvenstveno nucleus tractus solitarius (NTS), koji ima dodatne veze s jezgrama locus coeruleusa, parabrahijalnim jezgrama, te s jezgrama talamusa, hipotalamusa i amigdale. Navedeni mehanizmi vjerojatno omogućuju antiepileptički učinak VNS-a, kao i lokalne promjene u moždanom protoku i oslobađanju specifičnih neurotransmitera.
Nakon ugradnje VNS-a, uređaj se obično uključuje nakon 7 dana, a zatim se postupno povećavaju parametri stimulacije, najčešće za 0,5 mA svaka dva tjedna, do prosječne jačine stimulacije od oko 2,0 mA.
Drugi važni parametri VNS-a su trajanje stimulacije (ON time), koje obično iznosi 30 sekundi, te razdoblje bez stimulacije (OFF time), koje traje 5 ili 3 minute. Ostali parametri, poput širine pulsa i frekvencije stimulacije, obično su tvornički zadani i rijetko se mijenjaju, osim u slučaju nuspojava.
VNS je u početku bio namijenjen liječenju bolesnika sa žarišnom farmakorezistentnom epilepsijom, ali je kasnije indikacija proširena na generalizirane idiopatske epilepsije, kao i na bolesnike s određenim epileptičkim encefalopatijama, poput Lennox-Gastautovog sindroma, Dravetovog sindroma i drugih sličnih stanja. Također, VNS je odobren ne samo za odrasle već i za djecu stariju od 4 godine s farmakorezistentnom epilepsijom.
Učinkovitost VNS-a očituje se u smanjenju broja epileptičkih napadaja, u prosjeku za 40–50 %. Poznato je da se učinak VNS-a, kao i drugih neuromodulacijskih metoda, povećava s vremenom i trajanjem stimulacije. Uz to, VNS u nekim slučajevima može dovesti do smanjenja depresivnosti, poboljšanja raspoloženja i kvalitete sna, a u pojedinim studijama zabilježeno je i sveukupno poboljšanje kvalitete života.
Najčešće nuspojave terapije VNS-om su promuklost, kašalj, dispneja i lokalna bolnost na mjestu ugradnje uređaja. Te nuspojave su rijetke, javljaju se u 2–3 % slučajeva i obično su prolazne, najčešće nakon prilagodbe parametara stimulacije.
Vijek trajanja baterije VNS generatora obično je između 4 i 8 godina, ovisno o postavljenim parametrima, a nakon tog razdoblja bateriju je moguće zamijeniti.
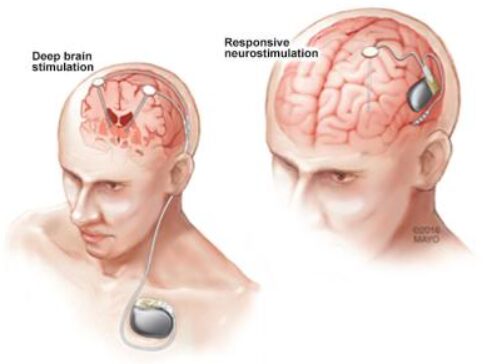
Duboka mozgovna stimulacija (DBS)
Responsivna neurostimulacija (RNS)
Duboka mozgovna stimulacija (DBS) metoda je koja se koristi u liječenju farmakorezistentne epilepsije.
Mehanizam djelovanja DBS-a temelji se na stimulaciji jezgri talamusa, prvenstveno anteriorne jezgre talamusa (ANT-DBS) i centromedijalne jezgre (CM-DBS). Anteriorne jezgre talamusa smještene su u prednjem dijelu talamusa i imaju snažne veze s hipokampusom, prednjim dijelom cinguluma i donjim dijelom parijetalnog režnja – regijama koje su dio limbičke i temporalne epileptogene mreže.
ANT-DBS pokazao je učinkovitost u liječenju žarišnih epileptičkih napadaja, s ili bez prelaska u bilateralne tonicko-kloničke napadaje (BLTKN). Najsnažniji dokaz učinkovitosti ANT-DBS dolazi iz prospektivne studije SANTE (Stimulation of the Anterior Nucleus of the Thalamus in Epilepsy), koja je pokazala više od 50 % smanjenja učestalosti napadaja u 54 % bolesnika, dok je kod 17 % bolesnika postignut šestomjesečni period bez napadaja nakon ugradnje DBS-a. Dugotrajno praćenje pokazalo je 69 % redukcije napadaja, uz 34 % smanjenja nuspojava uzrokovanih antiepileptičkom terapijom.
Druga moguća meta za stimulaciju putem DBS-a je centromedijalna jezgra talamusa (CMT). Stimulacija ove jezgre može dovesti do smanjenja generaliziranih epileptičkih napadaja te se pokazala učinkovitom i u liječenju bolesnika s epileptičkim encefalopatijama, poput Lennox-Gastautovog sindroma. Kao potencijalna ciljana područja za DBS navode se i jezgre nucleus accumbens te hipokampus.
DBS kontinuirano ili ciklički stimulira ciljane jezgre talamusa i ne ovisi o pojavi samog epileptičkog napadaja – stimulacija se odvija neovisno o napadu.
Kao moguće nuspojave primjene DBS-a navode se parestezije, osjećaj nelagode na mjestu implantacije uređaja te lokalne infekcije, koje se javljaju u 12–15 % slučajeva. Rijetko se mogu pojaviti psihijatrijski poremećaji poput depresije te smetnje memorije.
Responsivna neurostimulacija (RNS)
RNS sustav isporučuje električne impulse u određene regije mozga. Uređaj se kirurški implantira u točno određeno, manje područje mozga, nakon prethodne dijagnostičke obrade bolesnika s farmakorezistentnom epilepsijom, kod kojih su identificirana jedno ili dva epileptogena žarišta.
U odabrano područje implantira se uređaj sposoban za elektroencefalografsku detekciju početka napadaja, nakon čega slijedi stimulacija istog područja s ciljem prekida epileptičke aktivnosti. Ovaj je uređaj indiciran za bolesnike sa žarišnom epilepsijom koji imaju dva neovisna žarišta ili se žarišta nalaze u području elokventnog korteksa, poput motoričke ili govorne regije.
Za razliku od prethodna dva neuromodulacijska sustava, RNS aktivira stimulaciju reaktivno, tj. samo kada prepozna epileptičku aktivnost.
Učinkovitost RNS-a u liječenju farmakorezistentne epilepsije potvrđena je u više studija. Rezultati pokazuju 44 % smanjenja napadaja unutar godine dana, do 53 % nakon dvije godine, a kod 20 % bolesnika postignut je šestomjesečni period bez epileptičkih napadaja. Mnogi pacijenti s RNS-om također bilježe poboljšanja u određenim neuropsihološkim domenama, uključujući sposobnost imenovanja, verbalnu i vizualnu memoriju te izvršne funkcije.
Najčešće nuspojave RNS terapije uključuju infekciju na mjestu implantacije (2,6 %) i intrakranijalnu hemoragiju (2,1 %). Ukupna učestalost nuspojava nije veća nego kod ostalih neuromodulacijskih metoda.
Važno je napomenuti da pacijenti s ugrađenim RNS uređajem nisu kandidati za magnetsku rezonancu (MR) mozga.
Zaključak
Neuromodulacijske metode primjenjuju se kao palijativne opcije u liječenju farmakorezistentne epilepsije kod bolesnika koji nisu kandidati za resektivno neurokirurško liječenje.
Navedene metode pokazuju dobre rezultate uz relativno nizak profil nuspojava. Osim smanjenja učestalosti epileptičkih napadaja, korist neuromodulacijskih metoda očituje se i u poboljšanju kognitivnih funkcija i raspoloženja, kao i u ukupnom smanjenju mortaliteta.
Odabir neuromodulacijske metode ovisi prvenstveno o vrsti i karakteristikama epileptičkih napadaja kod pojedinog bolesnika. Ako postoji jedno žarište ili dva međusobno bliska žarišta, metoda izbora je RNS. U slučajevima s više žarišta, metoda izbora je VNS, dok se DBS preporučuje kada žarište epileptičkih napadaja nije jasno definirano.
U Hrvatskoj su za liječenje farmakorezistentne epilepsije trenutno odobrene metode VNS i DBS, dok RNS još uvijek nije odobren za uporabu u Europskoj uniji.
- The Vagus Nerve Stimulation Study Group. A randomised controlled trial of chronic vagus nerve stimulation for treatment of medically intractable seizures. The Vagus Nerve Stimulation Study Group. Neurology. 1995; 45:224-230
- Fisher, R ∙ Salanova, V ∙ Witt, T ∙ et al.. Electrical stimulation of the anterior nucleus of thalamus for treatment of refractory epilepsy. Epilepsia. 2010; 51:899-908
- Morrell, MJ, Group RNSSiES. Responsive cortical stimulation for the treatment of medically intractable partial epilepsy. Neurology. 2011; 77:1295-1304
- Salanova, V., et al., Long-term efficacy and safety of thalamic stimulation for drug-resistant partial epilepsy. Neurology, 2015. 84(10): p. 1017-25.
- Fan JJ, Shan W, Wu JP, Wang Q. Research progress of vagus nerve stimulation in the treatment of epilepsy. CNS Neurosci Ther. 2019;25(11):1222-1228. [DOI] [PMC free article] [PubMed] [Google Scholar]
- Hamilton P, Soryal I, Dhahri P, et al. Clinical outcomes of VNS therapy with AspireSR (including cardiac-based seizure detection) at a large complex epilepsy and surgery centre. Seizure. 2018;58:120-126. [DOI] [PubMed] [Google Scholar]
- Salanova V, Sperling MR, Gross RE, et al. The SANTÉ study at 10 years of follow‐up: effectiveness, safety, and sudden unexpected death in epilepsy. Epilepsia. 2021;62(6):1306-1317. [DOI] [PubMed] [Google Scholar]
- Yuan L, Zhang S, Liang S, Liu N, Yu X, Liang S. Deep brain stimulation of the anterior nucleus of the thalamus in a patient with super-refractory convulsive status epilepticus. Epileptic Disorders : International Epilepsy Journal with Videotape. 2019;21(4):379-384. [DOI] [PubMed] [Google Scholar]
- Tröster AI, Meador KJ, Irwin CP, Fisher RS, Group SS. Memory and mood outcomes after anterior thalamic stimulation for refractory partial epilepsy. Seizure. 2017;45:133-141. [DOI] [PubMed] [Google Scholar]
- Bergey GK, Morrell MJ, Mizrahi EM, et al. Long-term treatment with responsive brain stimulation in adults with refractory partial seizures. Neurology. 2015;84(8):810-817. [DOI] [PMC free article]
- Simpson HD, Schulze-Bonhage A, Cascino GD, Fisher RS, Jobst BC, Sperling MR, Lundstrom BN. Practical considerations in epilepsy neurostimulation. Epilepsia. 2022 Oct;63(10):2445-2460. doi: 10.1111/epi.17329. Epub 2022 Aug 9.
- Samanta D, Aungaroon G, Fine AL, Karakas C, Chiu MY, Jain P, Seinfeld S, Knowles JK, Mohamed IS, Stafstrom CE, Dixon-Salazar T, Patel AD, Bhalla S, Keator CG, Vidaurre J, Neuromodulation Strategies in Lennox-Gastaut Syndrome: Practical Clinical Guidance from the Pediatric Epilepsy Research Consortium. Epilepsy Res. 2025 Feb;210:107499. doi: 10.1016/j.eplepsyres.2024.107499. Epub 2025 Jan 2.
- Philippe Ryvlin , Sylvain Rheims , Lawrence J Hirsch , Arseny Sokolov , Lara Jehi Neuromodulation in epilepsy: state-of-the-art approved therapies 2021 Dec;20(12):1038-1047. doi: 10.1016/S1474-4422(21)00300-8. Epub 2021 Oct 25.
- Gouveia FV, Warsi NM, Suresh H, Matin R, Ibrahim GM Neurostimulation treatments for epilepsy: Deep brain stimulation, responsive neurostimulation and vagus nerve stimulation. Neurotherapeutics. 2024 Apr;21(3):e00308. doi: 10.1016/j.neurot.2023.e00308. Epub 2024 Jan 4
- Fisher RS. Deep brain stimulation of thalamus for epilepsy. Neurobiol Dis. 2023 Apr;179:106045. doi: 10.1016/j.nbd.2023.106045. Epub 2023 Feb 20
- Efremov F.A., Agaev R.V., Kim S.A., Moisak G.I., Anisimov E.D., Khabarova E.A., Rzaev J.A. Effectiveness of neuromodulation in patients with drug-resistant epilepsy after failed surgical treatment. Epilepsy and paroxysmal conditions. 2024;16(2):96-103. https://doi.org/10.17749/2077-8333/epi.par.con.2024.184



Komentiranje je dozvoljeno samo registriranim korisnicima. Svaki korisnik koji želi komentirati članke obvezan je prethodno se upoznati s Pravilima komentiranja na belupoint.hr.